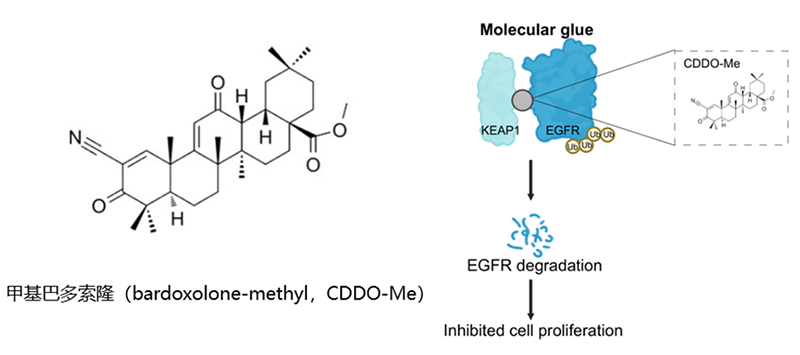
昆明动物所发现EGFR的分子胶降解剂
EGFR(epidermal growth factor receptor)在大多数肿瘤类型中高表达且驱动肿瘤的发生。然而,靶向EGFR的抑制剂仅在肺癌和结直肠癌中取得了良好的疗效,且仍会产生耐药性。EGFR抑制剂在其他多种肿瘤中均未见明显疗效,尤其在乳腺癌中收效甚微。基于此人们认为EGFR是乳腺癌及其它很多肿瘤中的不成药靶点。
中国科学院昆明动物研究所研究员焦保卫学科组总结过往文献认为EGFR抑制剂不敏感的机制主要与EGFR的降解受损有关。研究团队前期研究也发现了乳腺肿瘤中EGFR降解的一些重要调控因子,部分回答了乳腺癌对EGFR抑制剂不敏感的原因。事实上,无论 EGFR 是否突变,其降解异常都可成为其耐药产生的重要原因。因此,通过靶向 EGFR 降解异常来降低EGFR的水平是提高EGFR抑制剂临床疗效的重要手段。
靶向蛋白降解技术(targeted protein degradation,TPD)是解决致病蛋白靶点不成药的有效手段。TPD技术可通过机体自身的蛋白降解系统(包括泛素蛋白酶体系统和溶酶体降解系统)去除致病蛋白,因而比传统的小分子抑制剂拥有更广阔的应用潜力。分子胶水(molecular glue)是转化潜力大的一种TPD技术。研究团队发现三萜类化合物甲基巴多索隆(bardoxolone-methyl,CDDO-Me)可以同时直接与EGFR和E3泛素连接酶KEAP1结合,进而通过KEAP1将EGFR拉进E3泛素系统,最终进入自噬溶酶体降解。基于肿瘤原位移植模型和PDO模型(Patient-derived organoids),证实了CDDO-Me对三阴性乳腺肿瘤有良好的治疗效果。该研究发现了第一个EGFR的分子胶水,为CDDO-Me用于乳腺癌等EGFR抑制剂不敏感肿瘤类型的临床治疗打下重要基础。
近日,相关研究成果以Discovery of a molecular glue for EGFR degradation为题,在线发表于Oncogene,并同期获授权国家发明专利(ZL202210811615.7)。昆明医科大学与昆明动物所联合培养博士研究生王海瑞、昆明动物所副研究员王慧、陆军军医大学王睿为文章的共同第一作者。焦保卫、王慧、云南省肿瘤医院副院长聂建云和陆军军医大学乳腺甲状腺外科主任齐晓伟为文章的共同通讯作者。
该研究得到了科技部重点研发计划、国家自然科学基金委、中国科学院和云南省科技厅的资助。
文章链接:https://pubmed.ncbi.nlm.nih.gov/39627505/